

|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
PCR技术服务 环状DNA PCR技术服务 |
福建医科大学附属肿瘤医院邱素芳老师的研究团队主要研究方向为头颈部肿瘤的放化疗尤其是鼻咽癌的综合治疗。其科研团队利用label-free蛋白质谱的方法研究发现辐射的肿瘤细胞小胞外囊泡(外泌体)中包含一种新型的肿瘤相关抗原CDCP1(CUB domain-containing protein 1),并能被开发为可产生抗肿瘤免疫应答的肽疫苗。辐射的肿瘤细胞小胞外囊泡可以通过增强CD8 +和CD4 + T细胞的浸润而触发针对原发肿瘤和实验性肺转移的抗肿瘤免疫力。该研究成果刊登在学术期刊Theranostics (IF:8.579)上。(label-free蛋白质谱由康成生物丨数谱生物提供技术服务)
|
注:根据论文中对小胞外囊泡的描述,小胞外囊泡即是外泌体。为和原论文保持一致,本次解析使用“小胞外囊泡”。 康成生物丨数谱生物提供外泌体分离、外泌体鉴定、外泌体转录组学及外泌体蛋白组学等研究服务,欢迎咨询。
|
研究背景
放射治疗(Radiotherapy,RT)是目前癌症治疗的重要策略。越来越多的证据表明放疗在抗肿瘤免疫诱导中的作用。小胞外囊泡(Small extracellular vesicles ,sEVs)是在内小体网络中的囊泡体中形成的纳米囊泡(直径50-200nm),几乎所有类型的细胞都可以释放,包括癌细胞。 来源于供体细胞的sEVs通过交换其内容物(包括蛋白质、脂类和功能性遗传物质等)在局部及系统的细胞通讯中发挥着重要作用。肿瘤来源的sEVs作为天然肿瘤相关抗原(TAAS)的载体,可以有效的转移到树突状细胞(DCs)并诱导抗原特异性CD8+ T细胞活化。然而,辐射诱导的潜在机制、免疫系统的激活仍有待充分阐明。
在本研究中,作者研究了小胞外囊泡sEVs在RT诱导的抗肿瘤免疫中的作用。 照射8 Gy(Gy,剂量单位)的肿瘤细胞,通过超速离心法纯化sEV。在小鼠中建立了原发性肿瘤和实验性肺转移模型,以评估由sEV免疫引发的抗肿瘤免疫性。研究者进行了label-free蛋白质组学和生物信息学分析,以鉴定辐射引起的sEV中蛋白质组学的变化。辐射激活小胞外囊泡中共发现148个差异显著蛋白(fold change≥1.5,p ≤0.05),其中CDCP1表达水平显著升高。根据主要组织相容性复合体(MHC)I的结合和免疫原性,设计并合成了sEVs中上调蛋白衍生的肽作为疫苗。证明来自辐射的肿瘤细胞的sEVs可以通过增强CD8 +和CD4 + T细胞的浸润而触发针对原发肿瘤和实验性肺转移的抗肿瘤免疫力。辐射还可能使sEV充满肿瘤抗原和热激蛋白。此外,源自辐射诱导的sEV的CDCP1被鉴定为一种新型的肿瘤相关抗原,并被开发为可产生抗肿瘤免疫应答的肽疫苗。结果表明,使用辐射的肿瘤细胞分泌的sEV构成了肿瘤抗原传递和呈递的有效方法,该研究证明了小胞外囊泡在辐射触发的抗肿瘤免疫中的作用。
技术路线

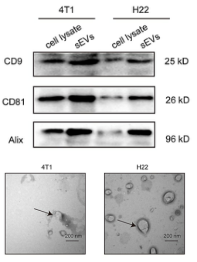
Figure 1. 小胞外囊泡的鉴定。Western blot检测小胞外囊泡的肿瘤特异性抗原CD9,CD61和Alix。电镜鉴定小胞外囊泡具有茶托状形态。
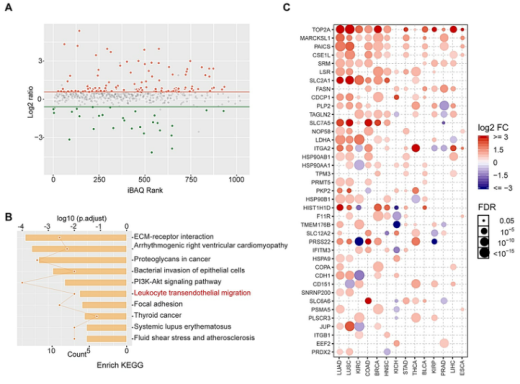
Figure 2. label free蛋白质谱和生信分析辐射诱导细胞上清小胞外囊泡的蛋白。
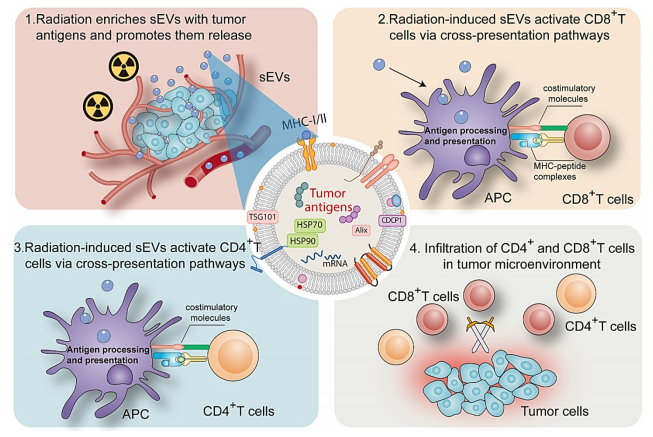
Figure 3. 辐射诱导的小胞外囊泡激活抗肿瘤免疫的机制。(1.辐射使含有肿瘤抗原的小胞外囊泡富集,并促进其从细胞内释放;2-3.这些辐射诱导产生的小胞外囊泡通过交叉呈递方式激活CD8+ 和CD4+ T细胞;4.CD8+ 和CD4+ T细胞浸润至肿瘤微环境发挥免疫作用)。
研究意义
本研究利用康成生物丨数谱生物的label-free蛋白质谱研究发现辐射的肿瘤细胞小胞外囊泡中含有一种蛋白CDCP1,它是一种新型的肿瘤相关抗原,并被开发为可产生抗肿瘤免疫应答的肽疫苗。辐射的肿瘤细胞小胞外囊泡可以通过增强CD8 +和CD4 + T细胞的浸润而触发针对原发肿瘤和实验性肺转移的抗肿瘤免疫力。
论文链接
相关技术服务

