

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
相关服务
相关产品
相关资源
外泌体(exosomes):
外泌体是活细胞经过"内吞-融合-外排"等一系列调控过程而形成的膜性囊泡,来源于晚期核内体(也称为多囊泡体 ),直径约为30-150nm,密度在1.13-1.21g/m1,天然存在于血液、唾液、尿液及母乳等体液中,同时外泌体也存在于组织和细胞间隙中。人体中几乎所有类型的细胞均能产生外泌体,人体中大约有1014个外泌体,大约平均每个细胞产生1000-10000个。
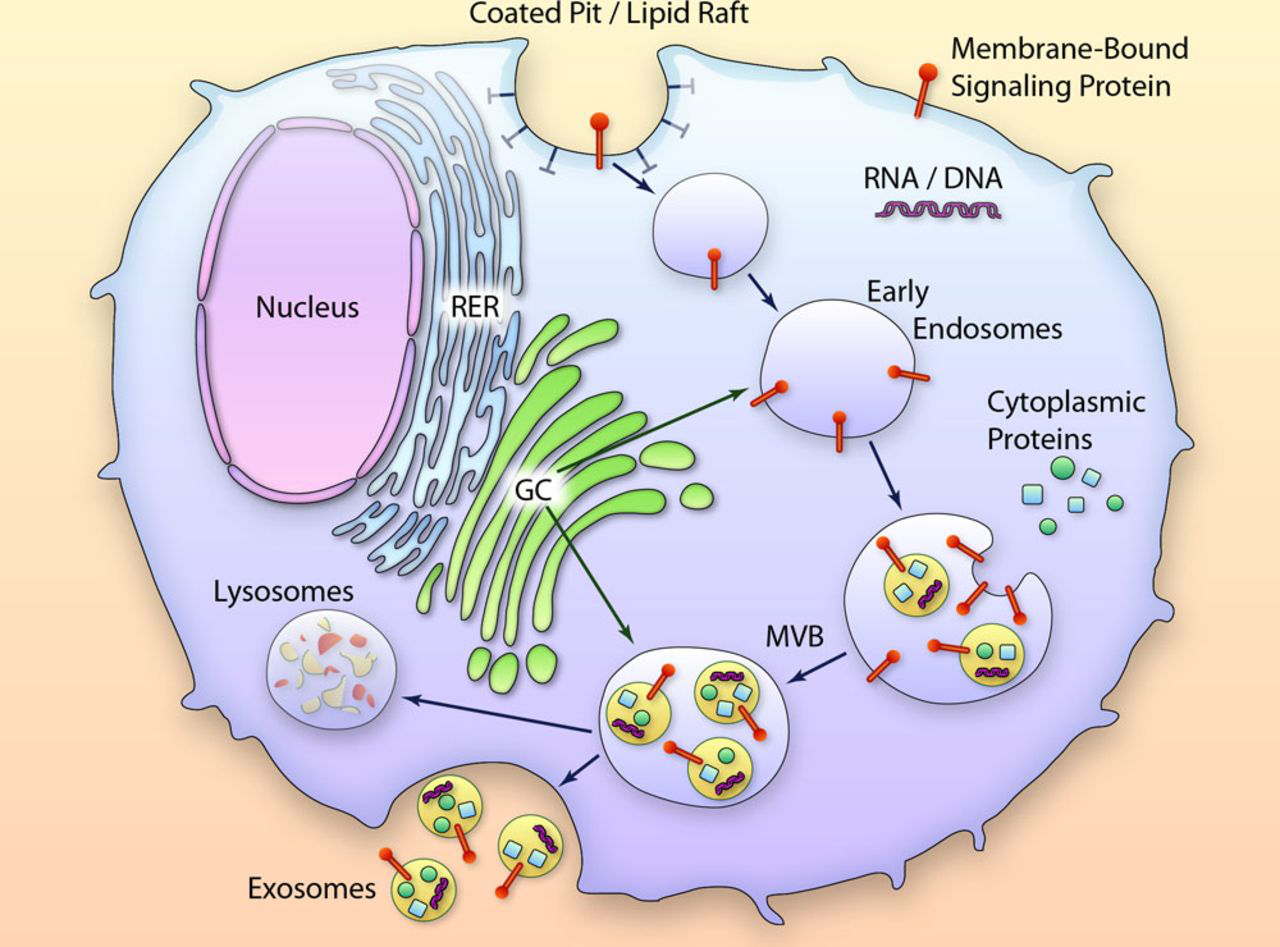
图1.外泌体的形成过程
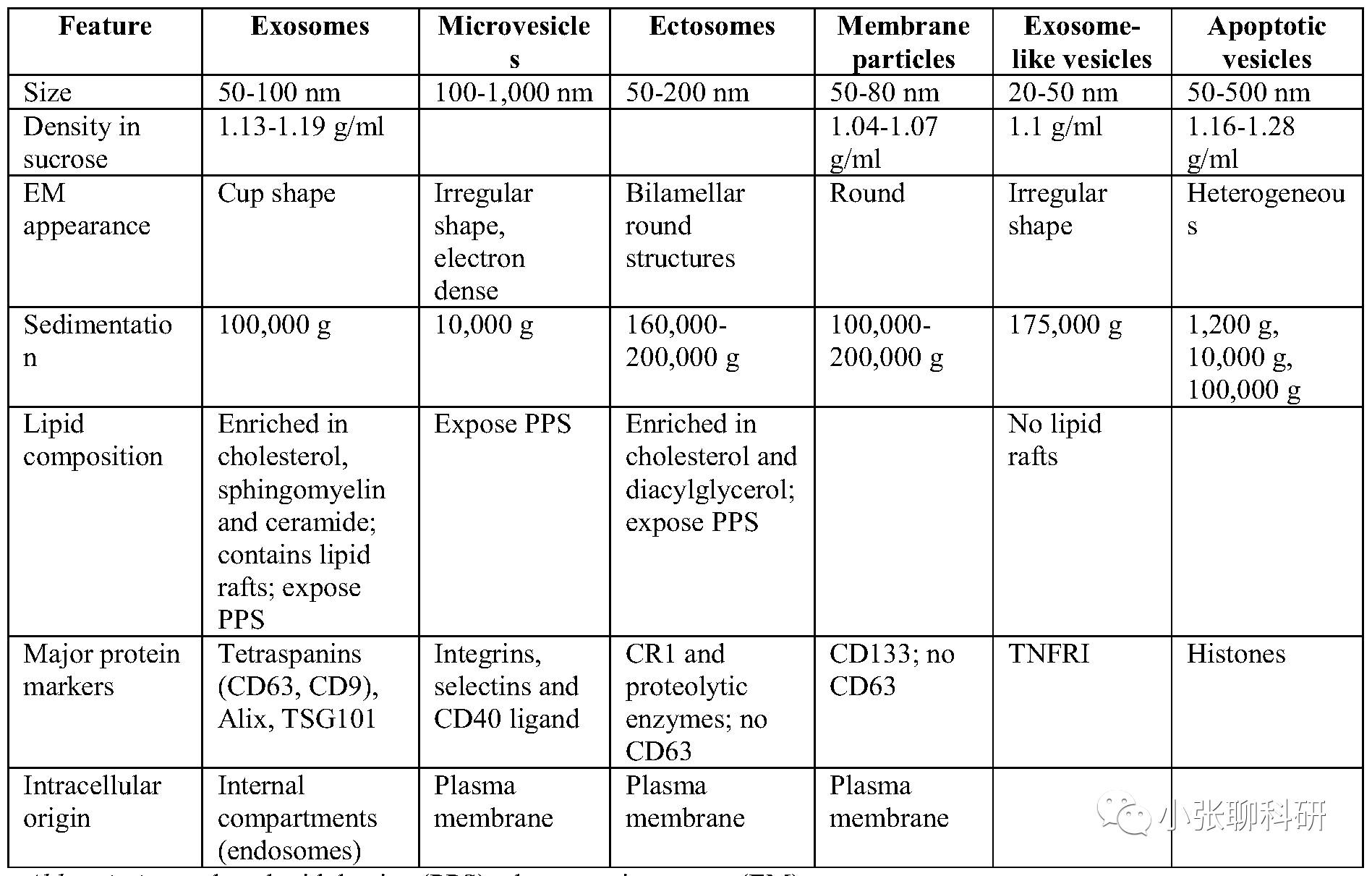
表1.外泌体与常见的囊泡颗粒的比较
外泌体的成分:
外泌体的膜与细胞膜相似,同为磷脂双分子层,外泌体膜上有脂质筏限制膜流动,参与包括跨膜信号转导、物质内吞、脂质及蛋白定向分选的多种功能。外泌体中含有核酸(miRNA、DNA、lncRNA、mRNA、tRF等),蛋白和脂类,在细胞间物质和信息转导中发挥着重要作用。
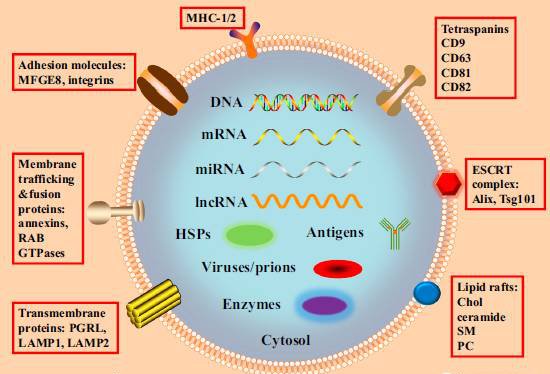
图2.外泌体的组成
外泌体的功能:
外泌体发挥功能主要通过两种方式:
1. 细胞-细胞之间的通讯,譬如抗原递呈,这是发挥功能的主要方式。
2. 垃圾中转站:将细胞或组织中多余的或者有害的分子排除,这为研究生物标志物提供了可能。
基于以上两种作用模式,外泌体在干细胞治疗、免疫调控、肿瘤转移和血管生成以及生物标志物等领域发挥着非常重要的作用。
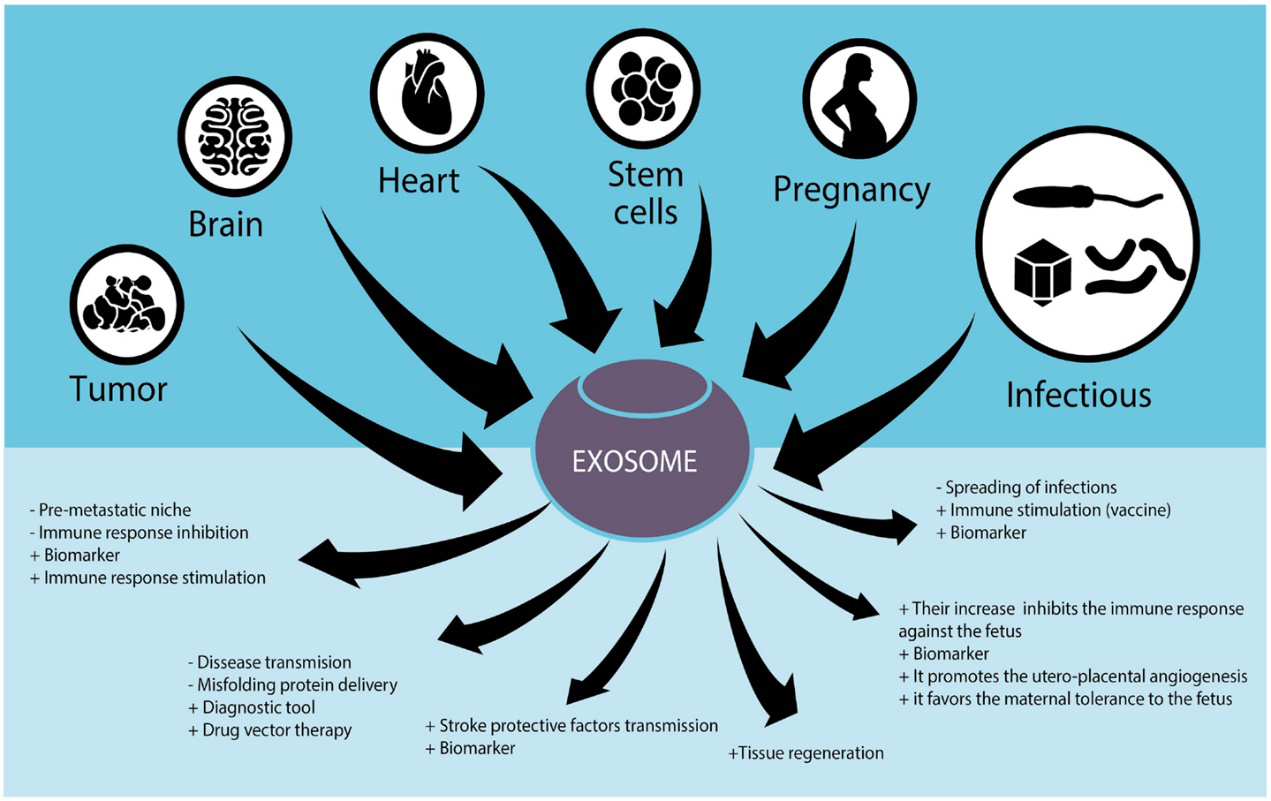
图3.外泌体的功能
为什么研究外泌体?
1. 揭示疾病发病机制:从微环境角度揭示细胞之间通讯促进疾病发生的原因
2. 寻找疾病诊断和预后的分子标志物
3. 外泌体作为药物载体,实现靶向给药
要研究外泌体,首先就必须获得外泌体。目前外泌体分离方法主要有以下几种:
| 分离方法 | 原理 | 优势 | 劣势 |
|---|---|---|---|
| 超速离心 | 利用差速离心的方法分别将细胞碎片、大的囊泡及其他的杂质去除,最后得到外泌体 | 常用的外泌体纯化手段,可分离到大小相近的囊泡颗粒。操作简单,获得的囊泡数量较多 | 对于血清血浆样本,分离效率较低,纯度不够。操作费时,回收效率不稳定 |
| 密度梯度离心 | 将超速离心与蔗糖密度梯度联合使用,根据外泌体的密度特性来进行分离纯化 | 得到的外泌体纯度高 | 周期长,操作繁琐,且此方法对超离的时间要求非常高。 |
| 色谱法 | 根据凝胶孔隙的孔径大小与样品分子尺寸的相对关系而对溶质进行分离的分析的方法 | 区分大的和小的囊泡,保持外泌体结构的完整性 | 一次处理一个样本,耗费时间较多,需要特殊的设备,应用不广泛 |
| 超滤 | 由于外泌体是一个大小约几十纳米的囊状小体,大于一般蛋白质,利用不同截留相对分子质量(MWCO)的超滤膜对样品进行选择性分离,便可获得外泌体 | 简单高效,且不影响外泌体的生物活性 | 从超滤膜上回收外泌体损失大,且在处理过程中外泌体结构遭到破坏 |
| 多聚物沉淀 | 聚乙二醇(PEG)为常用的多聚物,可与疏水性蛋白和脂质分子结合共沉淀,进而利用此原理分离外泌体 | 操作简单,快捷 | 纯度和回收率低,杂蛋白较多(假阳性),颗粒大小不均一,产生难以去除的聚合物,机械力或者吐温-20等化学添加物将会破坏外泌体 |
| 免疫亲和 | 外泌体表面有其特异性标记物(如CD63、CD9蛋白),用包被抗标记物抗体的磁珠与外泌体囊泡孵育后结合,即可将外泌体吸附并分离出来 | 特异性高、操作简便、不影响外泌体形态完整 | 效率低,外泌体生物活性易受pH和盐浓度影响,不利于下游实验 |
表2.外泌体分离方法的总结比较
鉴于目前的外泌体提取方法的各自的优缺点,Aksomics结合现有的方法以及相关的资料,开发出新的外泌体分离方法,与现有的方法相比具有以下优点:
1. 操作简单,快捷,对于血清血浆样本只需1.5-2h即可拿到外泌体
2. 纯度高:血液样本中高丰度污染蛋白含量非常低(对于蛋白组学实验特别重要)。

