|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
PCR技术服务 环状DNA PCR技术服务 |
eccDNA往往包含一些调控功能元件,例如增强子。这些携带增强子元件的eccDNA可以游离于基因组的不同区域,得以激活正常条件下不受这些元件调控的基因(图1),从而驱动这些基因表达变化并改变细胞功能,从而可能导致癌症等疾病的发生和发展[2]。
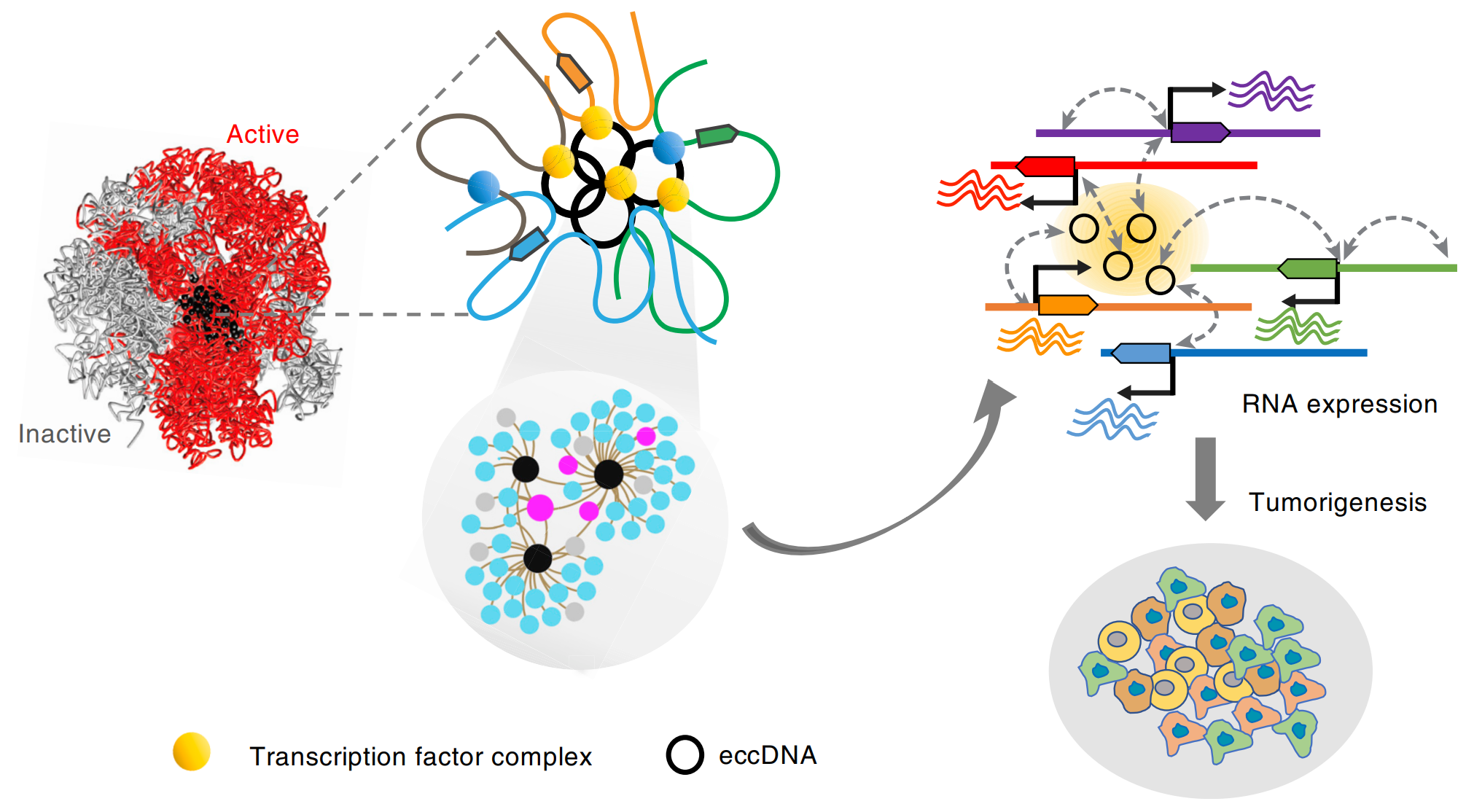
图1. eccDNA作为移动的增强子促进转录和肿瘤发生的模型
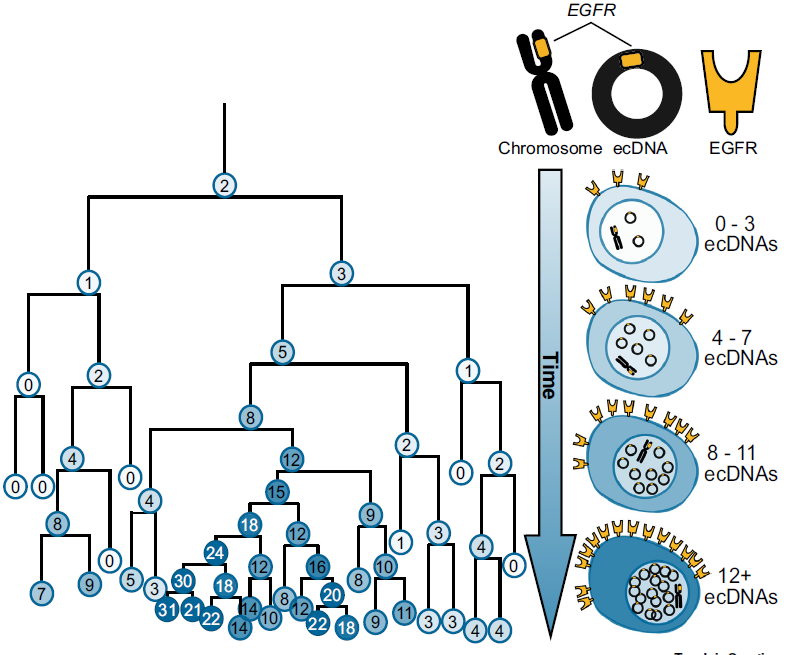
ecDNA是只存在于癌症中的大型具备克隆能力的环状DNA分子,小从10 kb到几兆碱基(Mb)不等,这些分子可以自我复制,但由于缺乏着丝粒而在有丝分裂中不均匀地遗传到子代细胞。这些ecDNA由于通常携带致癌基因和抗药性基因,能够为肿瘤组织的生长发展提供选择优势,并引起了肿瘤组织的遗传异质性,使治疗难度大大增加(图2),ecDNA的发现和鉴定是近年来癌症研究的重大突破与研究热点之一。
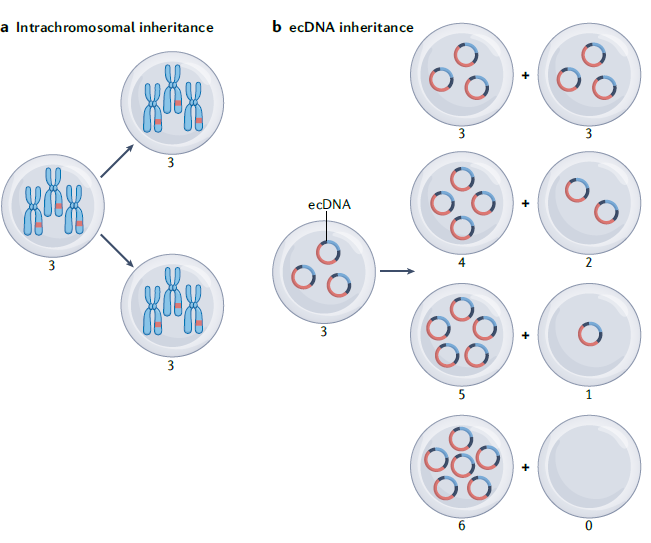
总的来说,环状DNA调控着多种多样的分子生物学机制和生理过程(图3),与多种疾病紧密相关(表1),是优良的诊断、预后标志物(表2)[5]。
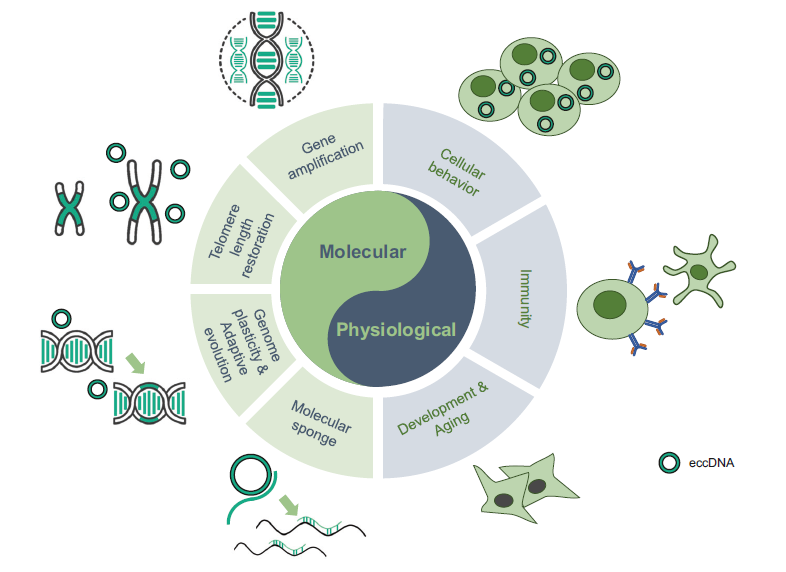
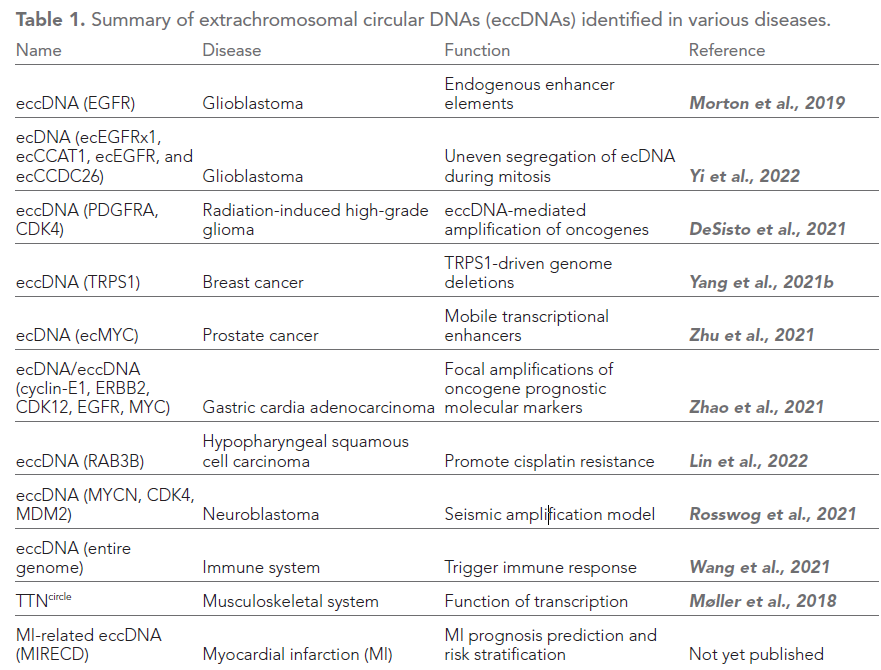
表1. 在各种疾病中发现的环状DNA[6]
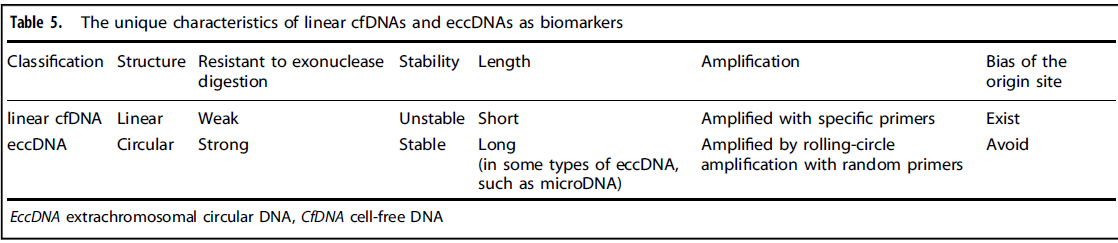
表2. 环状DNA作为生物标志物,比线性cfDNA更具优势[5]
参考文献:
1.Hung, K.L., P.S. Mischel, and H.Y. Chang, Gene regulation on extrachromosomal DNA. Nat Struct Mol Biol, 2022. 29(8): p. 736-744.
2.Zhu, Y., et al., Oncogenic extrachromosomal DNA functions as mobile enhancers to globally amplify chromosomal transcription. Cancer Cell, 2021. 39(5): p. 694-707.e7.
3.Noorani, I., P.S. Mischel, and C. Swanton, Leveraging extrachromosomal DNA to fine-tune trials of targeted therapy for glioblastoma: opportunities and challenges. Nat Rev Clin Oncol, 2022. 19(11): p. 733-743.
4.Nathanson, D.A., et al., Targeted therapy resistance mediated by dynamic regulation of extrachromosomal mutant EGFR DNA. Science, 2014. 343(6166): p. 72-6.
5.Yang, L., et al., Extrachromosomal circular DNA: biogenesis, structure, functions and diseases. Signal Transduct Target Ther, 2022. 7(1): p. 342.
6.Zhao, Y., et al., Extrachromosomal circular DNA: Current status and future prospects. Elife, 2022. 11.
线性染色体DNA和环状线粒体DNA的存在会导致环状DNA 测序结果中有效reads比例降低,因此有必要将二者去除。我们的环状DNA-Seq测序平台采用了限制性内切酶PacI对环状线粒体DNA进行切割,将其转化为线性DNA,然后使用线性DNA特异的外切酶将线性化的线粒体DNA以及染色体DNA消化,再使用滚环扩增的方式,将环状DNA进一步放大和富集,从而提高了测序质量。
实验流程
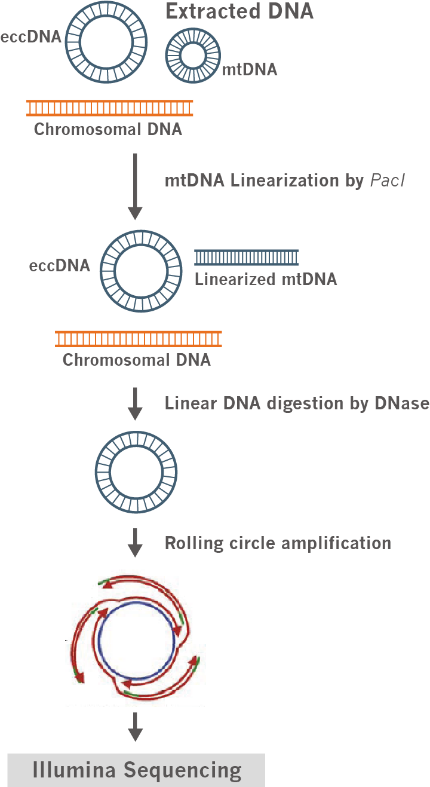
1.基因组DNA抽提;
2.PacI酶处理,线性化环状线粒体DNA;
3.DNA外切酶去除线性DNA;
4.滚环扩增环状DNA;
5.超声打断与DNA建库;
6.高通量测序;
7.数据分析;
8.提供实验报告。
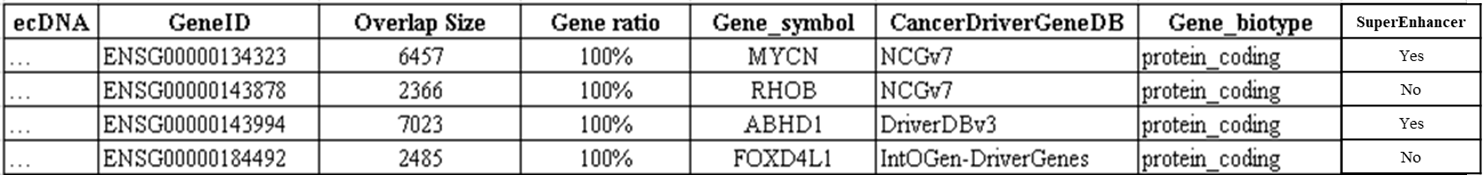
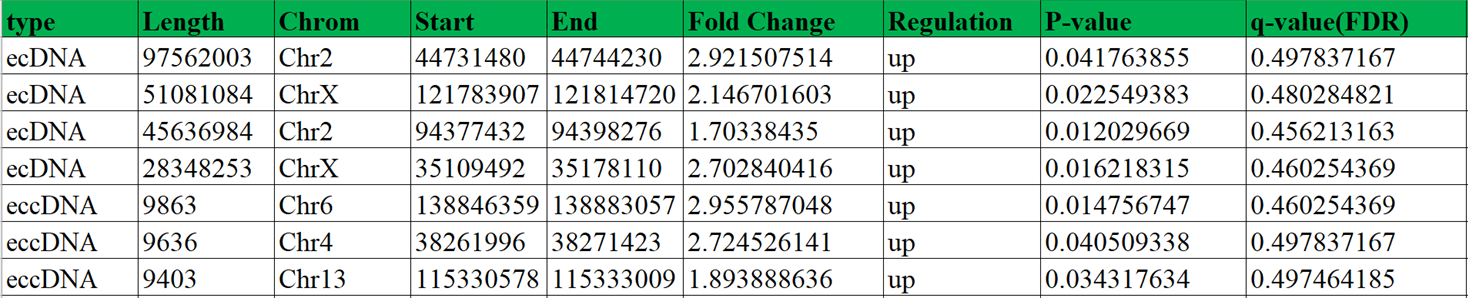
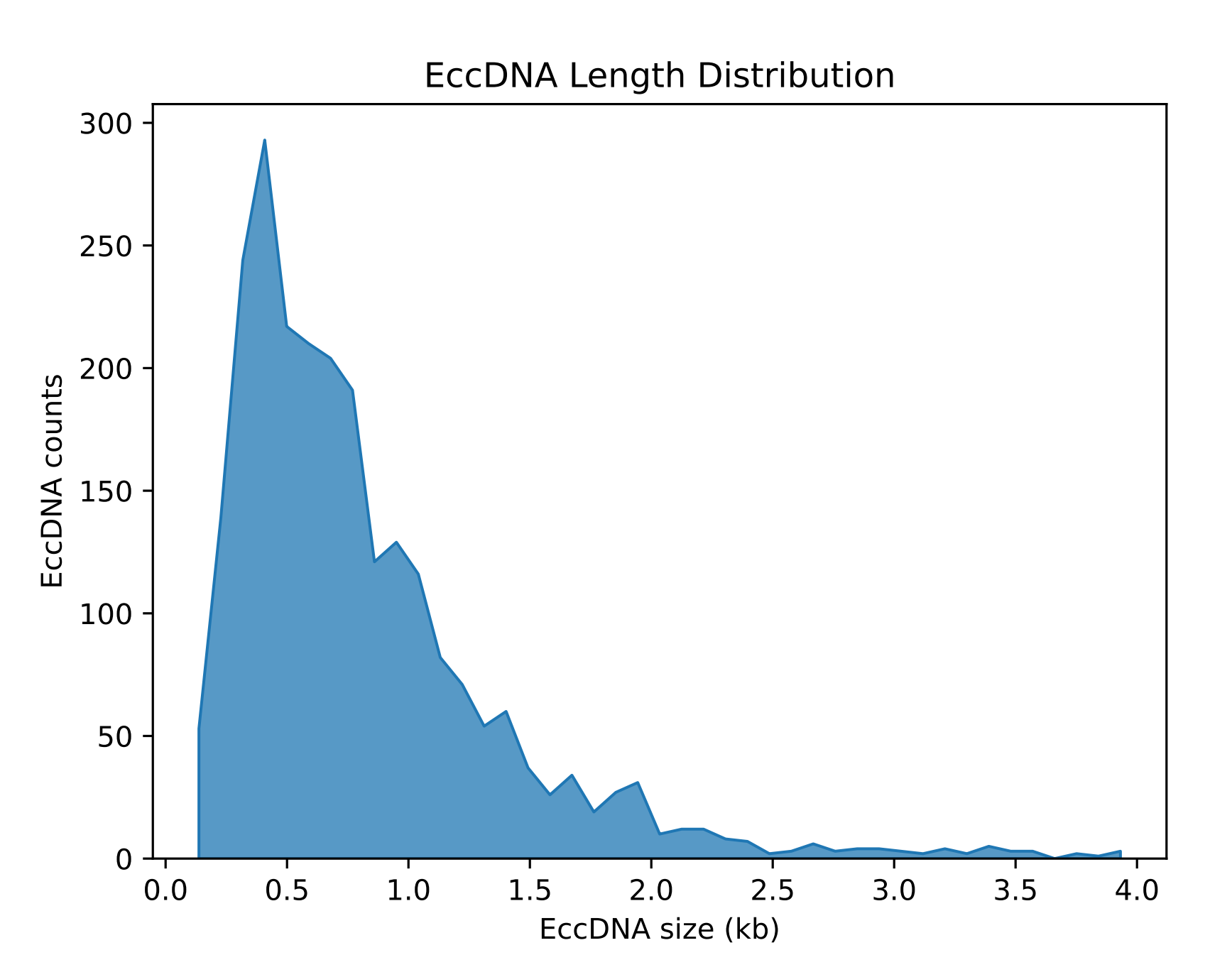
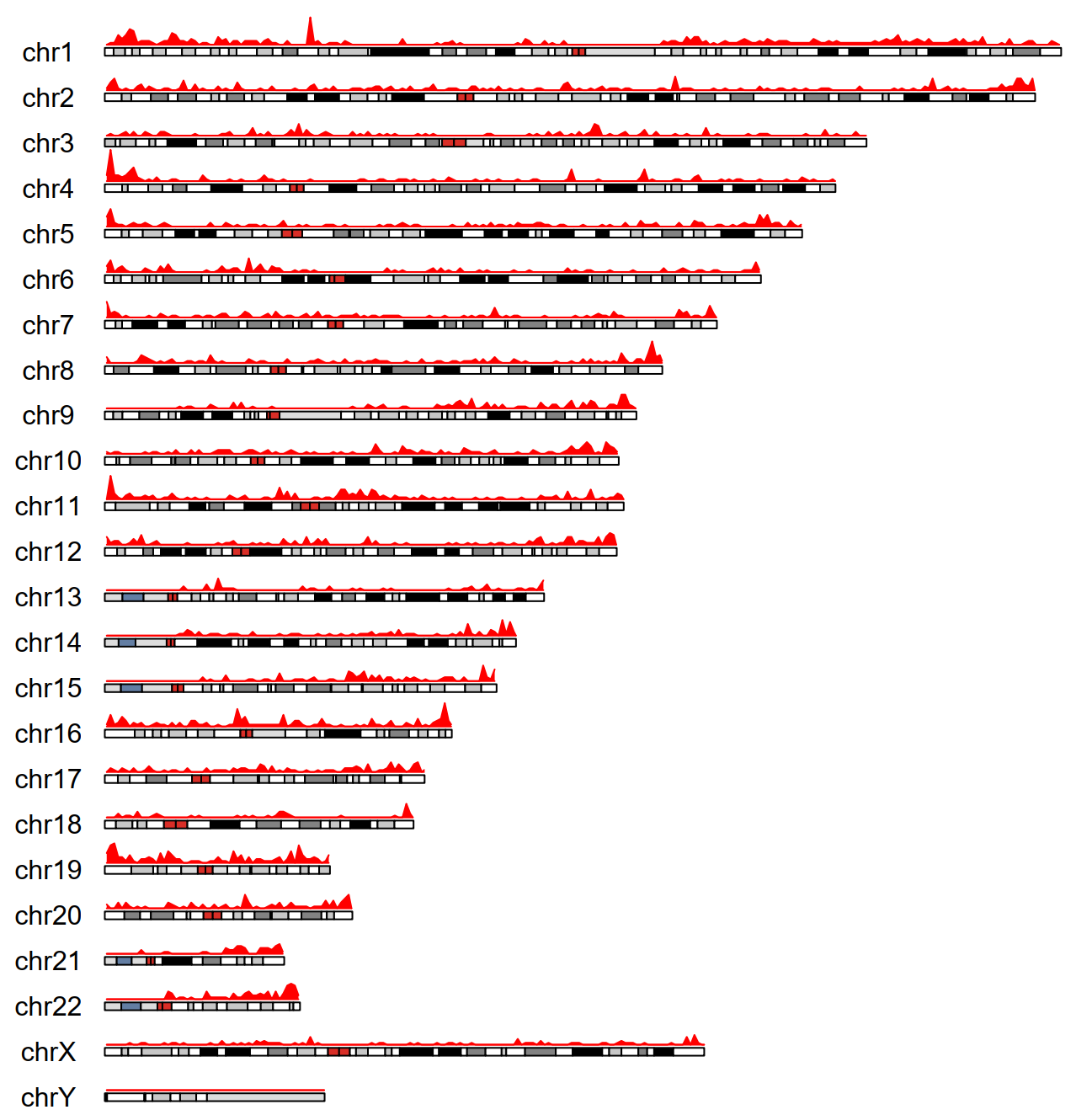
2.环状DNA长度和染色体分布统计图