

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
暨南大学附属第一医院徐安定教授长期致力于探索脑血管疾病在临床和基础研究中面临的各项重大问题及其解决方案。课题组采用Arraystar circRNA芯片筛选发现环状RNA分子circOGDH在急性缺血性卒中(Acute Ischemic Stroke, AIS)患者血浆外泌体和小鼠模型缺血半暗带脑组织(Penumbra Tissue,PEN)中显著上调。实验结果显示,AIS患者外周血中circOGDH的表达上调与缺血PEN组织的体积扩大呈正相关;在分子机制方面,作者发现缺氧急性期显著高表达的circOGDH能够靶向竞争结合miR-5112以促进下游靶基因COL4A4高表达,进而加重缺血条件下半暗带神经元的凋亡过程。这些发现提示circOGDH是一个AIS高敏感、高特异性的诊断生物标志物,且可能成为从分子层面精准判断缺血半暗带大小的的指标;该研究丰富了环状RNA参与缺血半暗带神经元损伤的机制,并为AIS的诊疗提供新的方向和潜在的药物靶点。
该研究成果于2022年发表在学术期刊Circulation Research上,影响因子为23.218(Arraystar circRNA芯片由康成生物|数谱生物提供技术服务)。

研究背景
急性缺血性卒中AIS是导致中国人群致残和致死的第一大病因。治疗AIS最重要的是在黄金时间窗口内重新疏通阻塞的血管,以挽救缺血的半暗带组织PEN,如果在这段时间内没有进行再灌注疏通,PEN将发展为不可逆转的梗死灶。但因为院前延误等多种客观因素,最终接受血管再通术的患者仍为少数,且血管再通后依然有近半患者预后不佳。因此,对AIS患者进行影像学之外的分子水平检测和评估PEN的存在、并据此采取针对性的干预对AIS患者急救有重要意义。环状RNA是一类环形非编码RNA,可通过外泌体等囊泡跨越血脑屏障传递中枢信号。已有研究表明,circRNA可以通过结合miRNA发挥基因表达的调控功能。目前有越来越多的研究发现,circRNA在AIS的发生发展中扮演重要的角色。因此,本文重点关注了circRNA作为生物标志物在AIS发病的参与以及在神经元损伤过程中的作用机制,为高效诊断AIS疾病进展程度和开发相应治疗方案提供了可靠的机制研究基础。
研究思路
文章着重于研究circOGDH在大脑动脉闭塞模型小鼠的PEN组织和45名AIS患者的血浆中的表达水平及其分子调控机制。作者运用Arraystar circRNA芯片检测发现AIS患者的血浆中circOGDH表达显著上调。进一步的PCR验证和脑损伤成像结果表明circOGDH表达水平与AIS患者PEN组织体积大小呈正相关。另外,作者还通过ROC曲线验证了circOGDH的表达水平与AIS发病严重程度和预后不良有关,能够作为诊断和预测AIS患者预后情况的生物标志物。这些结果表明circOGDH是调节缺血神经元活力的潜在治疗靶点,并且在外周血中富含神经元衍生的外泌体,在AIS患者中是良好的预测性生物标志物。
功能研究发现,在AIS小鼠模型中敲低circOGDH能够导致PEN体积缩减,显著减轻AIS的发展,并下调缺氧条件下神经元凋亡过程;而过表达circOGDH能够显著增加AIS小鼠模型的脑血管阻塞体积,加重疾病的进展。
在分子机制方面,作者通过AGO-RIP-PCR实验发现和验证在缺氧急性期显著高表达的circOGDH能够靶向竞争结合miR-5112以促进下游靶基因COL4A4高表达,进而加重缺血条件下半暗带神经元的凋亡过程,增加了神经元损伤,敲低circOGDH显著增强了缺血条件下的神经细胞活力。此外,作者同时发现脑中circOGDH可以通过外泌体释放到外周血中。总之,这些结果表明circOGDH能够以在外周血中外泌体形式存在,是诊疗AIS良好的生物标志物,并且在脑缺血条件下有助于调节神经元活力,是AIS的潜在治疗靶点。
技术路线

结果展示
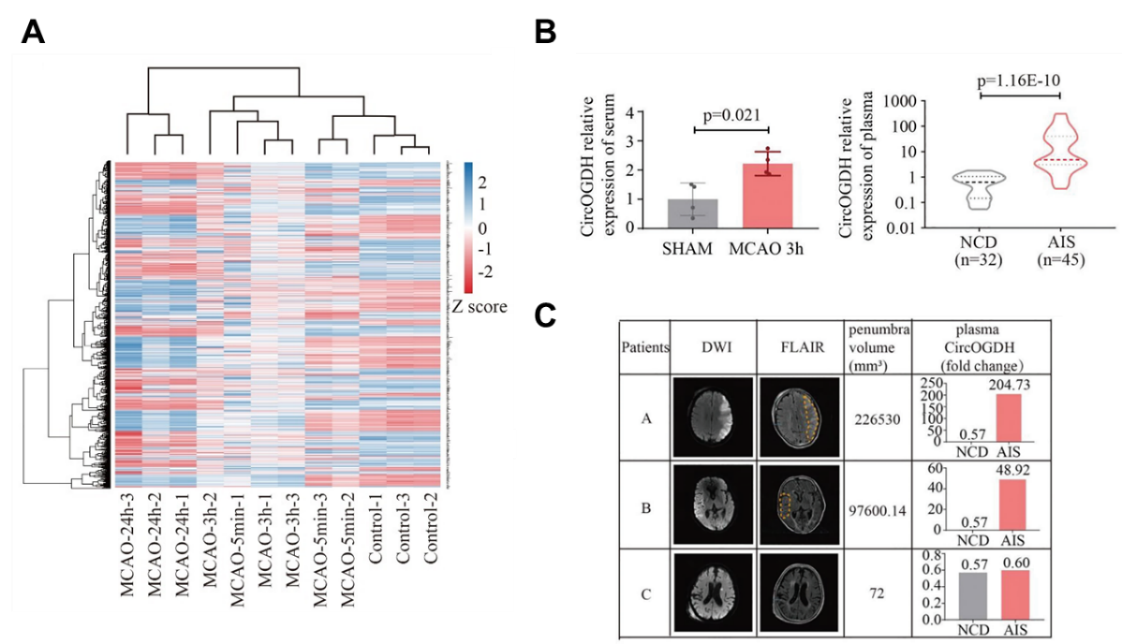
图1:circOGDH在AIS模型小鼠的外周血中显著上调。
A Arraystar circRNA芯片热图显示AIS模型小鼠与对照组的表达差异;
B qRT-PCR验证circOGDH在AIS模型小鼠与患者外周血中显著上调;
C qRT-PCR和影像学检验验证circOGDH表达水平与AIS患者PEN组织大小呈正相关。
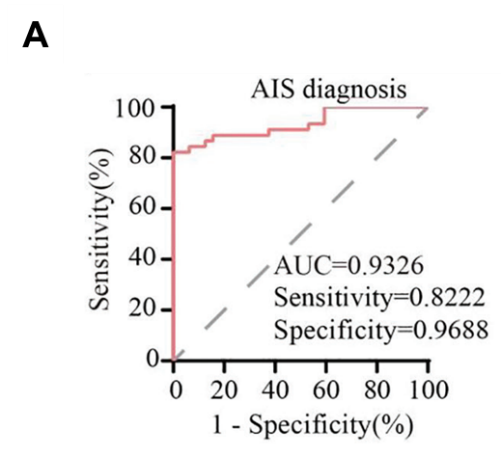
图2:biomarker研究,ROC曲线显示circOGDH可作为AIS疾病进展和预后的生物标志物。
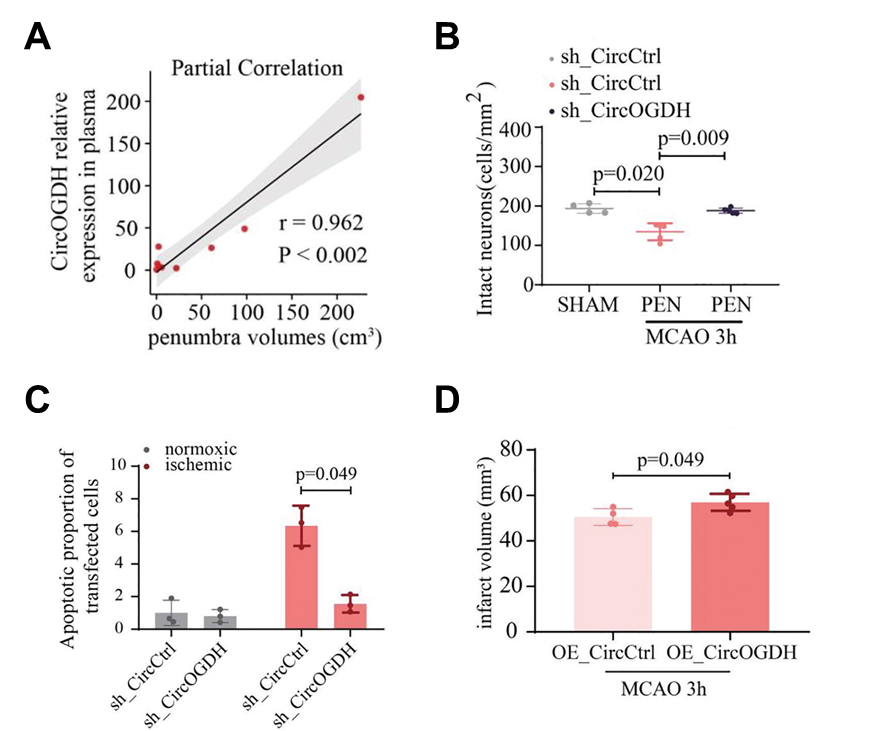
图3:功能研究,验证circOGDH表达水平对AIS疾病发展的影响。
A扩大样本验证circOGDH表达水平与AIS患者PEN组织大小呈正相关;
B敲低circOGDH显著缩减AIS小鼠模型PEN组织大小;
C敲低circOGDH显著降低AIS小鼠模型细胞神经元凋亡比例;
D过表达circOGDH显著增加AIS小鼠模型的脑血管阻塞体积。

图4:机制研究,circOGDH结合miR-5112并影响下游COL4A4基因的表达水平,最终调控神经元凋亡过程。
A AGO-RIP-PCR验证circOGDH可结合Ago2蛋白参与ceRNA调控机制;
B RNA Pull down-PCR验证circOGDH可结合miR-5112;
C过表达和敲低circOGDH、COL4A4验证circOGDH通过ceRNA调控机制影响下游效应基因COL4A4表达水平,并影响神经元凋亡过程。
研究意义
本研究使用Arraystar circRNA芯片在急性缺血性卒中AIS患者和小鼠模型中筛选,发现了环状RNA分子circOGDH表达水平显著上调。作者发现circOGDH在AIS患者的血浆和半暗带组织PEN中高表达,与PEN体积和AIS预后相关。通过体内外实验,作者证明了circOGDH能够通过与miR-5112结合,调控COL4A4的表达,影响缺血神经元的凋亡。此外,作者还发现circOGDH可以通过外泌体跨越血脑屏障,从而在外周血中作为AIS的生物标志物。这项研究揭示了circOGDH在AIS发病中的重要角色,为AIS的诊断和治疗提供了新的思路和靶点。
原文出处
https://www.ahajournals.org/doi/10.1161/CIRCRESAHA.121.319412
康成生物丨数谱生物可提供的相关技术服务
RIP-PCR

