

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
暨南大学汕头临床医学院王昊教授团队与暨南大学生命科学技术学院万钦黎教授团队、周庆华教授团队联合发表了名为“ALKB-1-dependent tRNA methylation is required for efficient paternal mitochondrial elimination”的研究性论文。该研究发现,去甲基化酶ALKB-1通过调控tRNA的m1A甲基化修饰,影响线粒体蛋白质稳态与ROS水平,进而介导父源线粒体的精准清除。这项研究首次将表观转录组修饰与线粒体质量控制、母系线粒体遗传三大生物学过程建立功能联系,为男性生育力下降及胚胎发育异常提供了潜在的分子解释路径。
该研究成果于2026年1月发表在学术期刊Nature Communications (IF: 15.7)上(数谱生物提供了文章所采用的 tRNA修饰测序技术服务与LC-MS tRNA修饰检测服务)。

研究背景
线粒体作为细胞的“能量工厂”,其DNA只通过母亲传递给后代,父源线粒体在受精后通常会被及时清除。母系线粒体遗传具有重要的进化意义,它可以阻止有害的mtDNA突变传播给后代,维持线粒体基因组的稳定性。tRNA修饰作为翻译的关键调控因子,已被证明可以影响蛋白质合成、细胞命运决定等多种生物学过程,但其在生殖和线粒体遗传中的功能尚未被充分探索。
研究思路
1. 筛选和鉴定调控父源线粒体清除的关键表观遗传因子
研究者选择秀丽隐杆线虫作为模型系统,对RNA和DNA修饰相关基因突变体进行系统筛选,结果发现ALKB-1突变体显示出明显的父系线粒体清除缺陷,从而锁定了候选基因。随后构建ALKB-1基因敲除和敲低模型,观察到精子中父系线粒体和线粒体DNA均出现异常积累,确认了ALKB-1的必要性。为了验证表型的特异性,研究团队进行了回补实验,发现重新表达ALKB-1能够挽救突变表型。最后通过组织特异性表达分析,发现ALKB-1确实在生殖细胞中高表达。
2. LC-MS tRNA修饰、tRNA修饰测序和RNC-seq高通量筛选揭示ALKB-1作用机制
为了探索ALKB-1调控父系线粒体清除的具体机制,研究者使用LC-MS tRNA修饰检测技术,结果显示ALKB-1突变体中m1A水平显著升高,而6mA水平没有显著变化,确认了ALKB-1的底物是m1A修饰,进一步的Dot blot实验证实了该结论。体外去甲基化实验表明,重组野生型ALKB-1蛋白能够显著降低茎环tRNA探针中的m1A修饰水平,而D247A突变体则无此活性。这些发现证明ALKB-1在父源线粒体中发挥tRNA m1A去甲基化酶活性。
为了进一步阐明ALKB-1在tRNA m1A修饰中的作用,研究者进行了tRNA m1A修饰测序分析。结果显示,ALKB-1D247A突变体中11种tRNA同工解码子的m1A水平显著升高,4种降低。进一步分析显示,上调的同工解码子中有9种胞质tRNA和2种线粒体tRNA,其中8种胞质tRNA为tRNA-Gly(TCC/GCC)同工受体,表明ALKB-1优先对tRNA-Gly进行m1A去甲基化。
研究者还进行了核糖体新生链复合物测序(RNC-seq)和蛋白质组学分析,以评估ALKB-1突变对翻译的影响。RNC-seq分析显示,与野生型N2相比,ALKB-1D247A线虫的翻译效率(TE)发生显著改变,471个翻译转录本上调,140个下调。蛋白质组学分析鉴定出ALKB-1D247A线虫中121个上调和47个下调的蛋白质。因此,研究者推断,m1A高甲基化导致tRNA构象改变和密码子识别异常,进而引起核糖体停滞,最终导致蛋白质翻译效率降低。
3. ALKB-1突变导致线粒体功能障碍
研究者通过透射电镜和活细胞成像观察嵴结构和网络完整性,发现ALKB-1突变导致线粒体结构异常。采用JC-1染色检测膜电位,荧光素酶法检测ATP产量,发现ALKB-1突变导致线粒体功能下降。使用MitoSOX和CM-H2DCFDA探针检测总活性氧和线粒体活性氧,发现ALKB-1突变导致线粒体ROS水平显著升高。通过蛋白质免疫印迹检测线粒体编码蛋白水平,发现ALKB-1突变导致线粒体蛋白合成减少。使用报告基因和定量PCR检测hsp-6、gro-1等分子伴侣表达,发现线粒体未折叠蛋白反应通路激活。进一步的遗传实验表明,ROS上升激活了氧化应激反应因子 SKN-1/Nrf2,并通过 ATFS-1 启动了线粒体未折叠蛋白反应,导致精子中线粒体和线粒体 DNA(mtDNA)的积累。这最终阻碍了父系线粒体的有效清除,并对雄性生育力及胚胎发育产生负面影响。
4. ALKB-1影响生殖功能
研究者在细胞水平进行精子竞争力分析,发现ALKB-1突变精子受精能力下降,直接影响生殖功能。从个体水平检测雄性生育力,发现后代数量减少且发育异常。在胚胎水平追踪早期胚胎发育,研究者发现ALKB-1突变导致父系线粒体延迟清除且胚胎致死率增加,带来母系遗传风险。进一步的进化水平跨代效应分析,发现线粒体DNA的异质性传递,影响种群遗传。
总之,正常情况下,ALKB-1活性正常维持tRNA m1A适度水平,保证翻译高效进行,线粒体功能健康,父系线粒体清除高效。当ALKB-1突变时,tRNA m1A高甲基化导致翻译受损,线粒体功能障碍,活性氧水平升高。此时一方面SKN-1激活发挥抗氧化防御的保护作用,另一方面ATFS-1激活导致线粒体未折叠蛋白反应和线粒体质量下降。两条通路共同作用最终导致精子线粒体清除缺陷和生育力下降。
技术路线
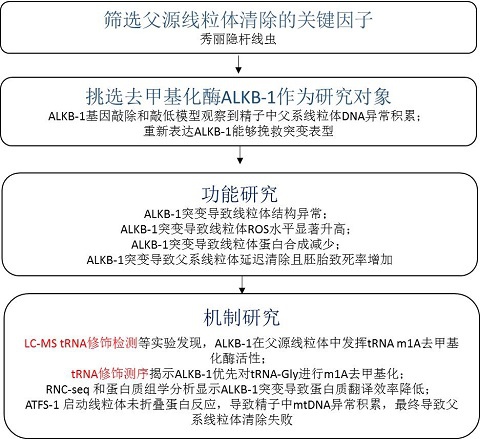
结果展示
1.去甲基化酶ALKB-1突变体显示出明显的父系线粒体清除缺陷。
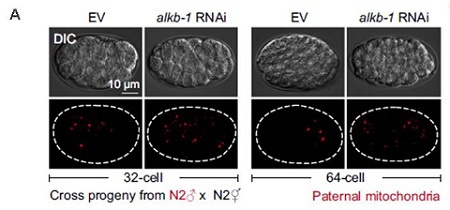
图1. A. 微分干涉对比(DIC)和 MTR 染色的父系线粒体图像显示敲低alkb-1导致父系线粒体明显增多。
2.ALKB-1 通过 tRNA m1A 修饰调节线粒体蛋白质稳态。
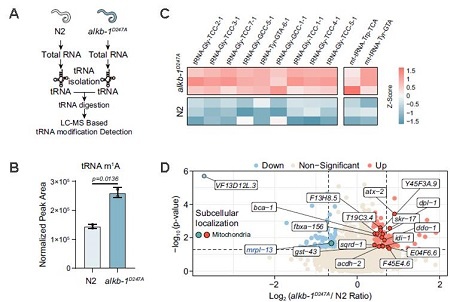
图2. A. LC-MS tRNA修饰检测流程图;B.LC-MS tRNA修饰检测结果显示,ALKB-1D247A突变体导致tRNA m1A总体水平显著上升;C. tRNA m1A修饰测序结果表明,ALKB-1D247A突变体中11种tRNA同工解码子的m1A水平显著升高;D. RNC-seq与蛋白组学分析结果显示,ALKB-1D247A突变体中线粒体蛋白明显增加。
3.ALKB-1突变导致线粒体功能障碍和胚胎发育受损。
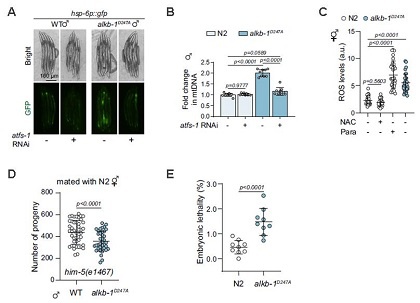
图 3. A. ALKB-1突变激活体线粒体未折叠蛋白反应通路;B. ALKB-1突变体中,ATF-1介导精子中线粒体 DNA(mtDNA)累积;C. ALKB-1突变导致线粒体ROS水平显著升高;D. ALKB-1突变导致怀孕数目显著减少;E. ALKB-1突变导致胚胎致死率增加。
4.去甲基化酶 ALKB-1 对父系线粒体消除(PME)调控作用的模式图。
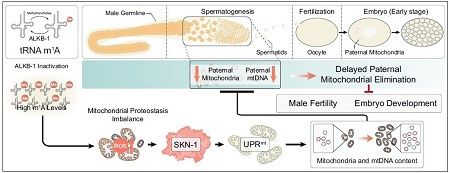
图 4. ALKB-1功能缺失会延迟秀丽隐杆线虫(C. elegans)中的父系线粒体清除(PME),这主要归因于其tRNA m¹A去甲基化酶活性。ALKB-1失活会升高tRNA m¹A水平,增强细胞质蛋白质翻译,从而增加线粒体蛋白质流入并导致功能障碍。这种破坏引发的活性氧(ROS)升高作为逆行信号的关键驱动因素,激活转录因子SKN-1和线粒体未折叠蛋白反应(UPRᵐᵗ)。该级联反应促进线粒体生物合成和线粒体DNA(mtDNA)扩增,在精子发生和早期胚胎发育过程中延迟父系线粒体的清除。
研究意义
该研究首次揭示了ALKB-1介导的tRNA m1A表观转录组修饰在父系线粒体清除中的关键调控作用。研究发现,ALKB-1通过其tRNA m1A去甲基化酶活性,调控线粒体蛋白质稳态,进而影响ROS产生、SKN-1/Nrf2激活和UPRmt诱导,最终调控父系线粒体清除效率。这一发现拓展了对tRNA修饰在生殖和线粒体遗传中功能的认识,揭示了表观转录组修饰与线粒体质量控制之间的密切联系。该研究还揭示了ALKB-1失活对雄性生育力和胚胎发育的负面影响,提示tRNA m1A修饰水平异常可能与不育和发育缺陷相关。鉴于ALKBH1在哺乳动物中的保守性,这些发现对于理解人类线粒体疾病和开发相关治疗策略具有重要参考价值。研究建立的“表观转录组-翻译-线粒体稳态-ROS-逆行信号”调控轴为深入理解母系线粒体遗传的分子机制提供了新的视角,也为未来研究线粒体疾病和开发创新治疗策略指明了方向。
文章原文
https://www.nature.com/articles/s41467-026-68813-6
康成生物丨数谱生物可提供的相关技术服务
LC-MS tRNA修饰检测
tRNA修饰测序-m1A/m3C/m1G/m2,2G

