

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
中山大学生命科学学院陈月琴教授和王文涛副教授作为共同通讯,在Cell Report发表名为“Chromatin-associated orphan snoRNA regulates DNA damage-mediated differentiation via a noncanonical complex”的研究性论文,该文章采用Arraystar snoRNA PCR芯片筛选发现急性髓系白血病AML细胞中染色质相关孤儿snoRNA(casnoRNA) SNORA73在多柔比星处理AML细胞导致DNA损伤压力时表达下调;功能研究发现SNORA73的下调可以维持基因组稳定性并抑制造血系统恶性肿瘤分化。机制研究发现,SNORA73的5’端非经典结构可以结合PARP1,通过与PARP1及H/ACA结合蛋白DKC1/NHP2形成SNORNP复合物来抑制PARP1的多聚ADP-核糖基化修饰PARylation(简称PAR修饰),进而影响癌基因组稳定性及肿瘤细胞分化。该研究成果于2022年发表在学术期刊Cell Report上,影响因子为9.423(snoRNA PCR芯片由康成生物|数谱生物提供技术服务)。

研究背景
小核仁RNA(snoRNA)主要定位于细胞核的核仁,根据结构的区别可以分为C/D box与H/ACA box两种不同类型。它们具有保守的序列特征,可以与小核仁核蛋白形成snoRNP复合物,进而为rRNA添加修饰,促进核糖体功能的正常运转。然而,有很大一部分 snoRNA(称为孤儿 snoRNA)缺乏rRNA修饰靶点且功能未知。孤儿 snoRNA 不与核仁中的 rRNA 配对,它们可能具有不同的亚细胞定位模式和非经典功能。
越来越多的研究揭示snoRNA在各种恶性肿瘤中异常表达,可调控癌症进程。其中一项泛癌研究表明,有76种snoRNA具有临床相关性。且在造血过程中,一部分snoRNA的表达具有发育和谱系特异性。此外,在包括以分化阻滞为特征的急性髓系白血病 (AML) 在内的造血系统恶性肿瘤中也观察到特定 snoRNA 的下调。由于snoRNA介导rRNA修饰并促进翻译的经典功能,对癌细胞的高增殖率至关重要,因此snoRNA的下调不太可能通过发挥其经典功能而促进癌症发展,snoRNA很可能在肿瘤转化过程具有非经典的新功能。
研究思路
snoRNA高通量筛选
Doxorubicin多柔比星处理可诱发DNA损伤压力,文章分离了多柔比星处理前后AML NB4细胞的细胞核质和染色质相关组分,分别进行Arraystar snoRNA PCR芯片筛选,根据差异倍数>2,P值<0.05发现203个snoRNA在染色质组分富集,命名为染色质相关snoRNA(casnoRNA),其中56个casnoRNA没有预测到rRNA靶点,属于孤儿casnoRNA。通过比较多柔比星处理前后的孤儿casnoRNA,发现SNORA73下调且在细胞和临床样本中qPCR验证趋势相符。
In vitro功能研究发现,SNORA73敲低可抑制DNA损伤及ATRA诱导的AML细胞分化并恢复癌细胞的克隆形成能力。In vivo功能研究发现,SNORA73敲低增加了小鼠骨髓、外周血、肝和脾脏的白血病细胞浸润并抑制了骨髓和外周血的白血病细胞分化。
机制研究发现,SNORA73 5’端形成非经典H/ACA box结构,tRSA pulldown和RIP实验证明SNORA73 5’端非经典结构可以结合PARP1蛋白。PARP1 是一种 ADP-核糖聚合酶,可催化多聚ADP-核糖基化,既可以修饰自身,也可以修饰其他蛋白质。 PARP1 自身 PAR修饰对于诱导 DNA 损伤应激后启动 DNA 损伤修复至关重要。FLAG-PARP1 CO-IP等实验证明PARP1通过SNORA 73结合DKC1/NHP2抑制自身PAR修饰,进而影响癌基因组稳定性和DNA损伤介导的分化。
技术路线

结果展示
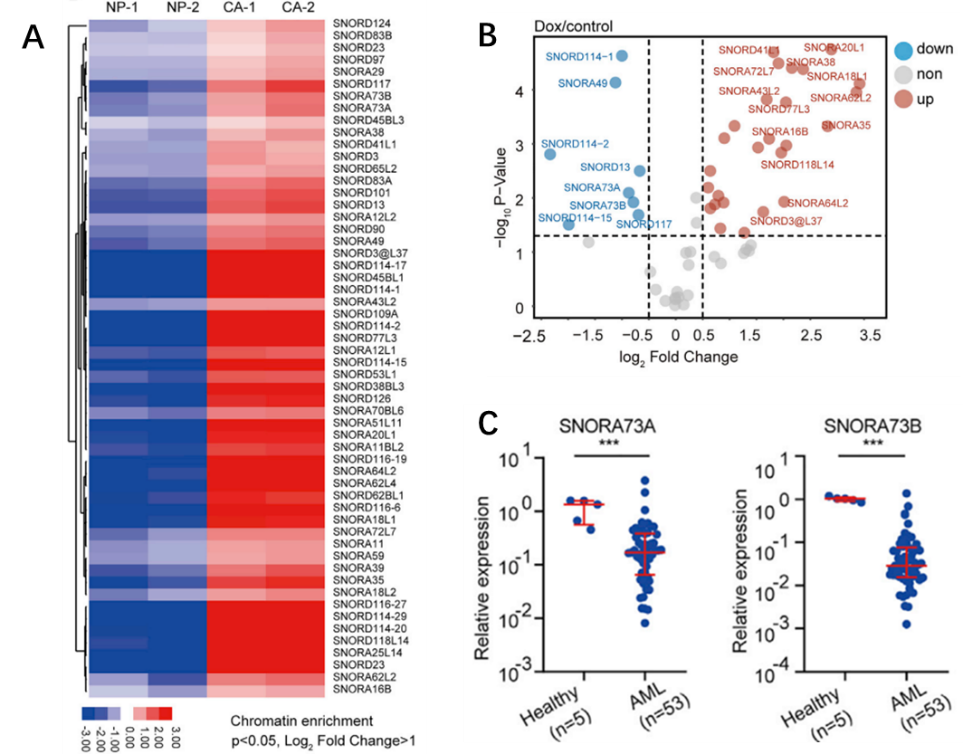
图1: snoRNA芯片显示染色质相关组分中SNORA73富集且在多柔比星处理后下调。
A Arraystar snoRNA PCR芯片热图显示AML细胞NB4染色质相关组分CA中部分casnoRNA富集;
B 多柔比星处理前后火山图显示上下调casnoRNA;
C 临床样本qPCR验证SNORA73在AML病人中显著下调。
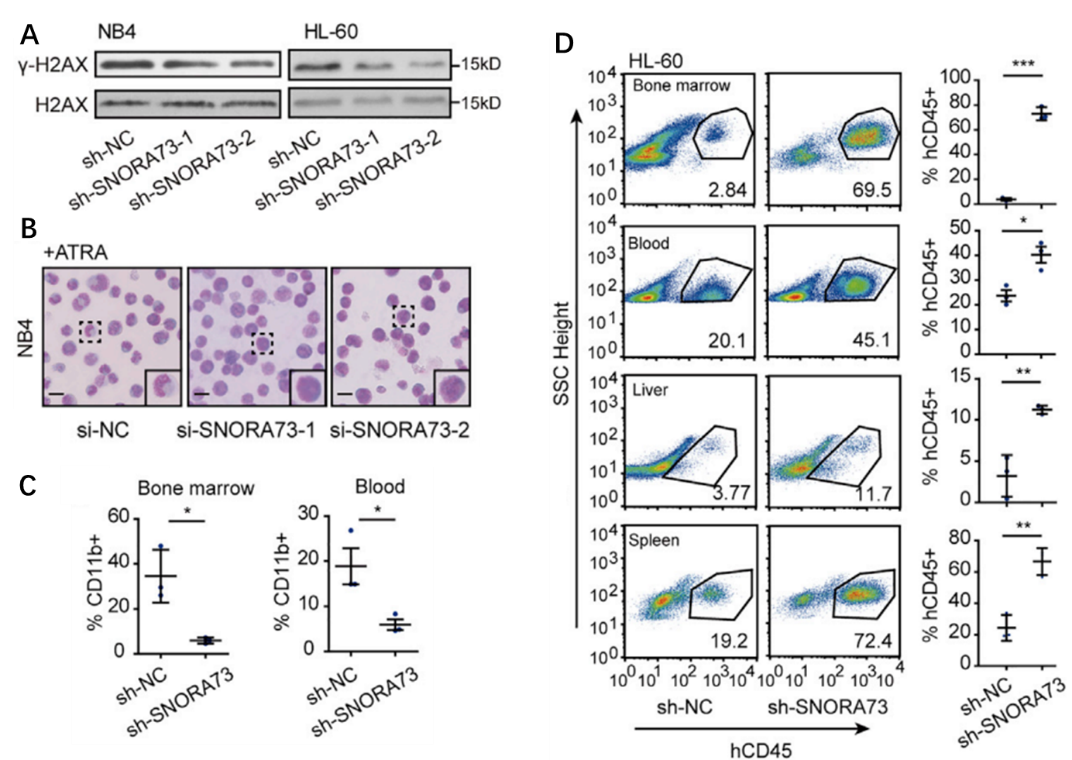
图2:In vitro和in vivo功能研究发现,SNORA73敲低可以维持基因组稳定性并抑制AML分化。
A In vitro SNORA73敲低可抑制DNA损伤(γ-H2AX:DNA损伤marker);
B In vitro SNORA73敲低可抑制ATRA诱导的AML细胞分化;
C In vivo SNORA73敲低可抑制小鼠骨髓和外周血中白血病细胞的分化能力;
D In vivo SNORA73敲低增加了小鼠骨髓、外周血、肝和脾脏的白血病细胞浸润。
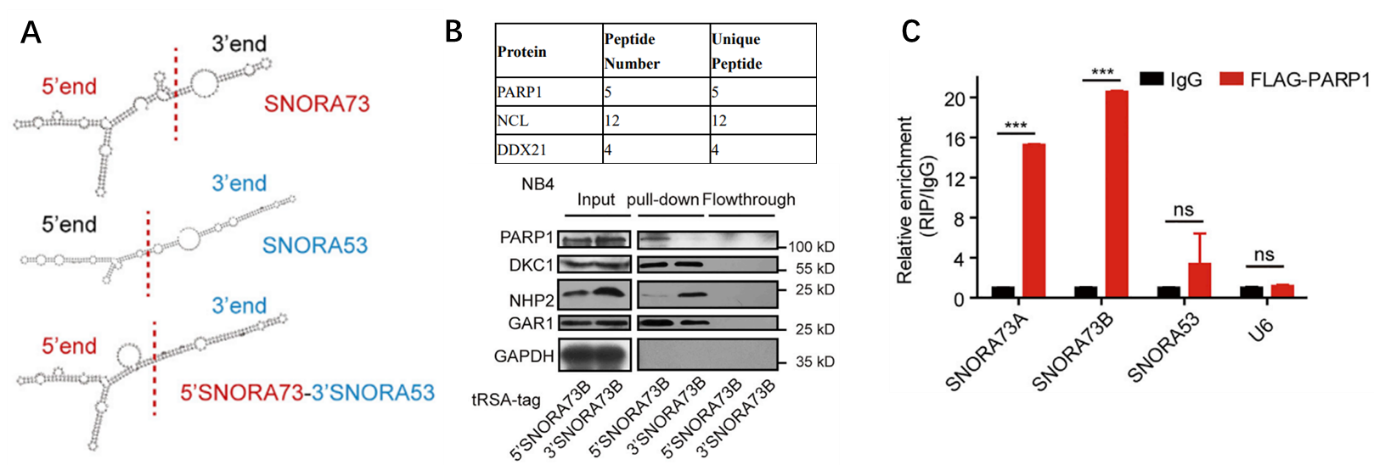
图3:机制研究证实SNORA73 5’ 端非经典结构可以结合PARP1。
A与经典H/ACA box SNORA53相比,SNORA73 5’端具有非经典结构;
B tRSA pulldown-MS及WB验证发现,SNORA73 5’端非经典结构可以结合PARP1;
C PARP1 RIP-PCR反向证明PARP1结合SNORA73。
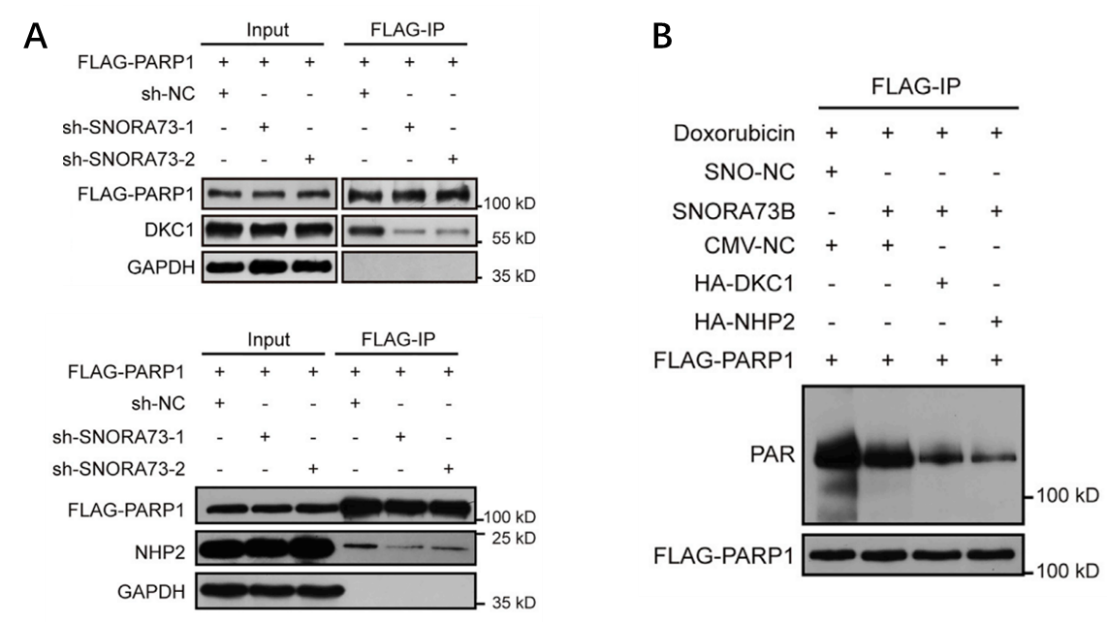
图4:机制研究证实PARP1及H/ACA结合蛋白DKC1/NHP2形成复合物来抑制PARP1的PAR修饰。
A Flag-PARP1 Co-IP实验证明PARP1可以结合DKC1/NHP2;
B Flag-PARP1-IP WB实验证明PARP1结合DKC1/NHP2抑制自身PAR修饰;
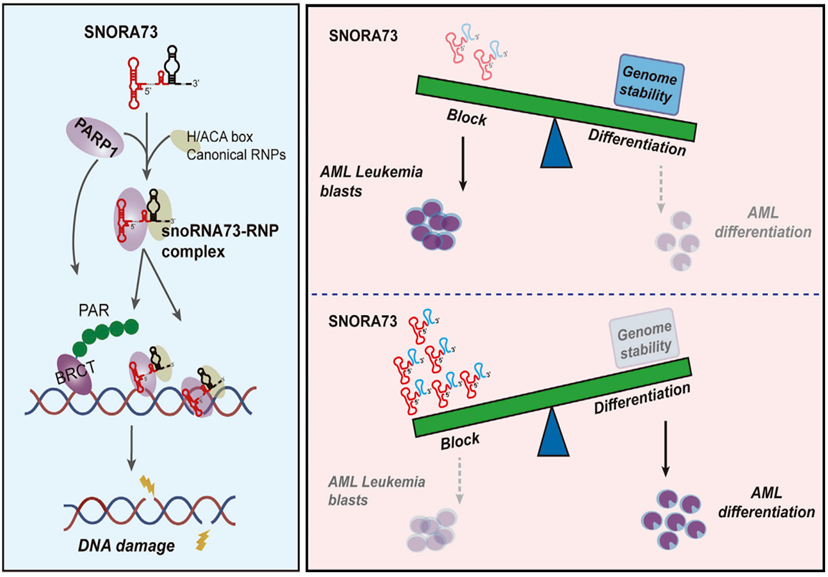
图5:作用机制图,在DNA损伤压力下SNORA73从染色质释放,通过与PARP1及H/ACA结合蛋白DKC1/NHP2形成SNORNP复合物来抑制PARP1自身的PAR修饰,进而影响癌基因组稳定性和DNA损伤介导的分化。
研究意义
本研究使用Arraystar snoRNA PCR芯片筛选发现多柔比星处理诱导的DNA损伤压力下,染色质相关的孤儿snoRNA SNORA73表达下调,且在AML病人中表达下调。功能研究发现SNORA73的下调可以维持基因组稳定性并抑制AML细胞分化。机制研究发现,SNORA73 通过与PARP1及DKC1/NHP2形成非经典复合物来抑制PARP1自身的PAR修饰,进而影响癌基因组稳定性及肿瘤细胞分化。这项工作揭示了孤儿casnoRNA的作用,并强调了snoRNA非经典结构与其功能多样性的联系,为snoRNA研究提供了新的思路与方法。
原文出处
康成生物丨数谱生物可提供的相关技术服务
Arraystar nrStar™ snoRNA PCR芯片
snoRNA RT-qPCR
RIP-PCR

