

|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
PCR技术服务 环状DNA PCR技术服务 |
一、G-loop的发现与定义

二、G-loop的动态调控机制
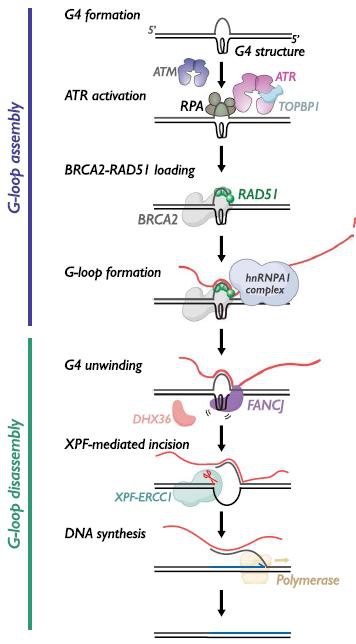
1.组装阶段
RNA同源入侵:由hnRNPA1复合物介导的RNA转录本(非实时转录产物)通过同源引导入侵G4互补链。DNA损伤响应:ATM/ATR激酶激活后,BRCA2-RAD51复合物在单链区域加载,促进RNA杂交。
DNA修复合成:切割触发DNA合成,最终将G4区域转化为标准双链。
G-loop循环缺陷导致小鼠干细胞中21,045个G4位点异常积累,引发R-loop滞留、复制叉停滞及DNA双链断裂。这一机制解释了BRCA2突变个体易患癌症的深层原因——G4失控性损伤。
长非编码RNA(lncRNA)丰度差异决定不同G4位点的动态性,为表观遗传调控提供新视角。
靶向DHX36/FANCJ可调控G4稳定性,为神经退行性疾病和早衰症提供干预思路。
G-loop机制的发现革新了对基因组结构动态性的认知:
跨周期调控:将转录后调控(RNA库存)、DNA损伤响应(ATM/ATR)、修复通路(BRCA2-RAD51)耦联为统一网络。
论文信息:Sato et al. (2025). Science [DOI: 10.1126/science.adr0493]
相关服务:
G-loop检测 (G4&R-loop Cut&Tag)
