

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
中科院生物物理研究所的范祖森教授课题组主要从事肿瘤干细胞、免疫细胞发育分化及肿瘤靶标发现与肿瘤个体化治疗等领域的研究,近期其团队利用Arraystar Mouse CircRNA Array研究了小鼠骨髓细胞(BM)中分离的长期造血干细胞(LT-HSCs)和多能干细胞(MPPs)的circRNAs表达谱。研究筛选出一个在LT-HSCs细胞核高表达的circRNA cia-cGAS,通过一系列功能机制实验发现LT-HSCs中cia-cGAS可以与DNA敏感的cGAMP合酶cGAS相互结合并抑制了其酶活性,阻碍cGAS结合基因组DNA,从而不能激活I型干扰素(IFN)的表达,维持LT-HSCs的静息状态。该研究同时也发现cia-cGAS是cGAS介导的自身免疫相关的有效抑制剂,为有效防治自身免疫性疾病与血液系统恶性肿瘤提供了新思路和潜在药物研发靶标。研究成果2018年发表在国际知名学术期刊Immunity(IF=22.845)。(芯片实验由康成生物提供技术服务)
研究背景
长期造血干细胞作为潜能最高的干细胞系,具有最高的更新和分化能力,可以为短期造血干细胞、多能干细胞等提供了持续性细胞补给。大多数时候,LT-HSCs处于休眠的静息状态,其干性的维持受转录因子及骨髓内环境等多种因素的影响,比如TNF、CXCL4和I型IFN等,然而LT-HSCs在静息状态与激活状态之间的精细调控机制尚未完全解析。研究思路
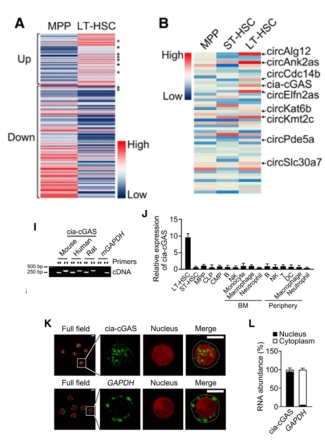
首先作者通过Arraystar Mouse CircRNA芯片分析了小鼠骨髓中分离的LT-HSC与MPPs的circRNAs表达谱,筛选出156种差异表达的circRNAs, qPCR验证结果与芯片一致。shRNA慢病毒转染发现,只有D430042O09Rik基因转录的circRNA cia-cGAS可以影响LT-HSCc的亚群分布。随后作者通过qPCR、Northern blot、核质分离及原位杂交实验发现cia-cGAS在LT-HSCs的细胞核内高度表达。

研究意义
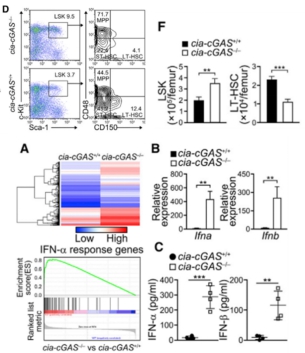
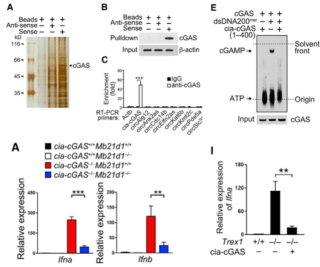
本研究通过Arraystar Mouse CircRNA Array筛选出一个LT-HSCs细胞核高表达的circRNA cia-cGAS,功能机制实验发现LT-HSCs中cia-cGAS可以与DNA敏感的cGAMP合酶cGAS结合抑制其酶活性,阻碍cGAS结合基因组DNA,从而不能激活I型IFN的表达,维持LT-HSCs的静息状态。同时cia-cGAS是cGAS介导的自身免疫相关的有效抑制剂,为有效防治自身免疫性疾病与血液系统恶性肿瘤提供了新思路和潜在药物研发靶标。
