

|
基因芯片技术服务 Small RNA芯片 piRNA芯片 染色质small RNA芯片 基因下游RNA(DoG RNA)芯片 lncRNA芯片 circRNA芯片 |
NGS测序技术服务 tRNA测序 tRF&tiRNA测序 miRNA测序 snoRNA测序 染色质small RNA测序 RNA测序 |
PCR芯片技术服务 nrStar™ ncRNA系列PCR芯片 NuRNA™ mRNA PCR芯片 |
PCR技术服务 lncRNA-qPCR circRNA-qPCR miRNA-qPCR tRF&tiRNA-qPCR mRNA-qPCR |
|
单细胞测序技术服务 靶向单细胞测序(lncRNA&mRNA) 单细胞测序 |
|
蛋白表达定量 DIA定量蛋白质组学 Label free非标定量 |
蛋白修饰定量 N-糖基化蛋白组学 O-GlcNAc修饰蛋白质组学 |
|
Ribo-seq Ribo seq(ribosome profiling) |
核糖体-新生肽链复合物(RNC) RNC联合 circRNA芯片 RNC联合 lncRNA芯片 RNC-seq |
|
NGS测序技术服务 环状DNA测序(eccDNA测序) |
第二军医大学免疫所所长、中国医学科学院院长曹雪涛院士课题组主要从事天然免疫与免疫调节基础研究、免疫治疗应用研究。近期其实验室用Arraystar CircRNA芯片研究发现circMTO1可以作为microRNA的吸附海绵结合癌基因miR-9从而上调p21的表达从而抑制肝细胞癌(hepatocellular carcinoma, HCC)的生长。该研究成果刊登在国际顶级期刊肝脏病学Hepatology(影响因子11.71)上。(芯片实验由数谱生物提供技术服务)
研究背景
肝细胞癌HCC是人类常见的恶性肿瘤之一,在恶性肿瘤发病率排在第五位。由于早期诊断困难和对各种治疗反应差,肝细胞癌的5年死亡率仍较高。尽管近年在肝癌的早期诊断和肝癌治疗等方面的研究取得了很大的进展,肝癌的治疗手段仍然是有限的。非编码RNA在癌症生物学中起到重要的作用,提供潜在的肝癌治疗靶点。一些内源性的非编码RNA如circRNA,在发育、细胞功能和特定的病理学应答中起到重要作用,特别是circRNA可以作为microRNA海绵来调控基因表达。研究失调的circRNA和它们在癌症中的功能引起越来越多的重视。
研究思路
为了研究circRNA在肝细胞癌中的表达及功能。研究者运用Arraystar Human circRNA芯片研究在7例肝癌组织和7例正常肝组织中circRNA的差异表达,筛选出肝细胞癌中20个差异显著的CircRNA做聚类分析(其中10个circRNA上调,10个circRNA下调),qPCR验证了这20个circRNA与芯片结果一致。circMTO1 (has_circRNA_0007874/has_circRNA_104135)在HCC组织中显著下调。相对于正常肝组织,circMTO1在87.4%(228/261)的肝癌组织中表达显著下降,并且与HCC病人的恶性程度相关。通过Miranda预测circMTO1能结合99个microRNA;FISH和RIP验证生物信息学预测结果circRNA可以和miR-9结合。过表达或敲除实验表明circMTO1会影响肝细胞癌的增殖,体内实验也证实了这一结果。LOF/GOF circMTO1发现circMTO1可以作为microRNA的吸附海绵结合癌基因miR-9从而上调p21的表达,抑制HCC的生长。因此,低表达的circMTO1可以作为预后诊断biomarker和潜在的HCC病人治疗的靶点。
技术路线
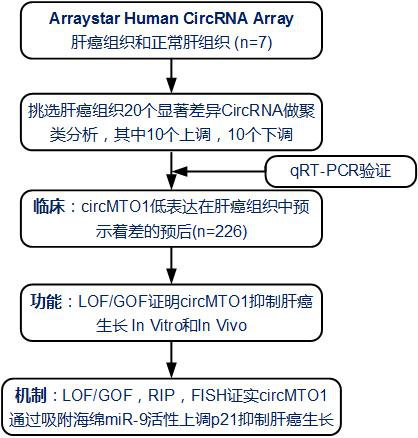
结果展示
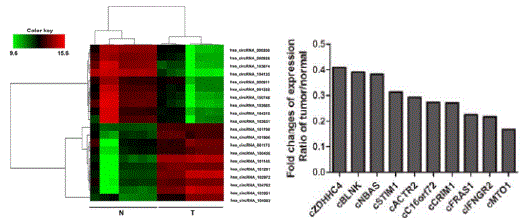
图1:挑选肝癌中20个差异显著的CircRNA做聚类分析;qPCR验证circMTO1芯片结果和qPCR结果一致。
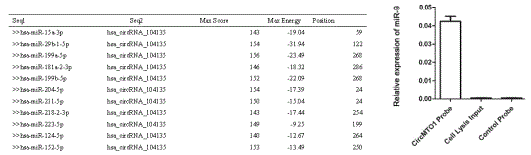
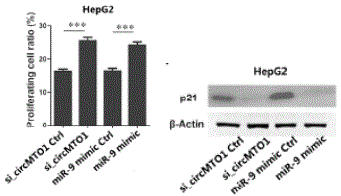
图3:circRNA通过microRNA海绵吸附miR-9上调p21的活性抑制肝癌
研究意义
本研究运用Arraystar CircRNA 芯片研究肝癌组织中的表达和功能。发现circMTO1的表达在HCC组中显著降低,并且与HCC病人差的预后相关。功能和机制研究发现,circMTO1通过海绵吸附miR-9,上调p21的表达抑制HCC的生长,意味着circMTO1在HCC的发育过程中起着抑癌基因的作用。进一步说,体内干预circMTO1实验表明circMTO1有HCC靶向治疗的潜力。结果表明circMTO1或可作为预后的诊断标志物和HCC治疗的靶标。
原文链接
Han D, Li J, Wang H, et al. Circular RNA MTO1 acts as the sponge of miR‐9 to suppress hepatocellular carcinoma progression[J]. Hepatology, 2017.

